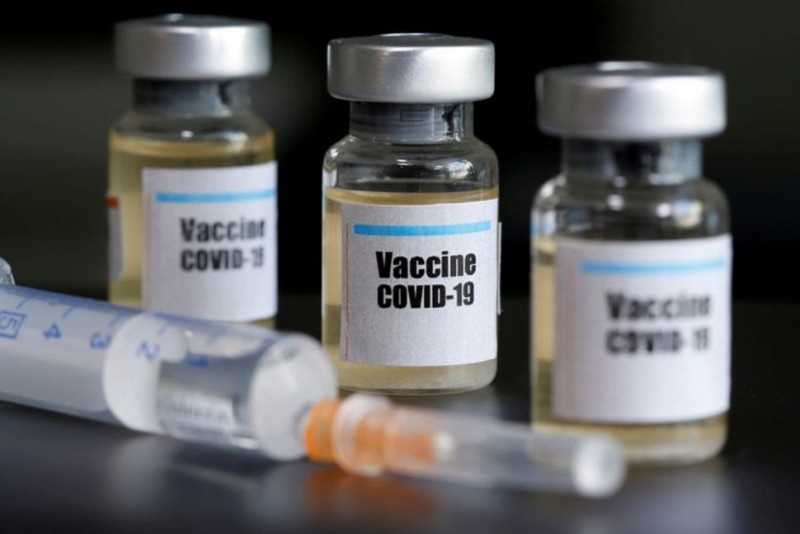
Moderna 冠狀病毒疫苗試驗的早期結果表明,受試者産生了針對該病毒的抗體

【美南新聞記者泉深報道】Mordrrna 生物技術公司5月18日宣布,接受Moderna 與美國國立衛生研究院(NIH) 合作開發的Covid-19疫苗的受試者産生了針對該病毒的抗體,早期取得了積極的結果。
Moderna首席醫學官塔爾·紮克斯(Tal Zaks)博士對CNN表示,如果未來的研究進展順利,該公司的疫苗最早將于明年1月份向公衆提供。
紮克斯說:“這絕對是好消息,我們認爲許多人已經等待了很長一段時間。”

這些早期數據來自1期臨床試驗,該試驗通常研究少數人群,重點研究疫苗是否安全並引發免疫反應。
這項由NIH領導的研究結果尚未經過同行評審或發表在醫學期刊上。
根據世界衛生組織的數據,總部位于馬薩諸塞州劍橋的Moderna是全球八家針對新型冠狀病毒疫苗進行人類臨床試驗的開發商之一。輝瑞公司(Pfizer)和Inovio公司也在美國,另外兩家在英國牛津大學,四家在中國。
Moderna 已爲數十名研究參與者接種疫苗,並在其中八名中進行了抗體測量。據該公司稱,所有八名參與者都對病毒産生了中和抗體,其水平達到或超過了從Covid-19自然恢複的人所見的水平。
中和抗體與病毒結合,使其無法攻擊人類細胞。
紮克斯說:“我們已經證明這些抗體,這種免疫反應,實際上可以阻斷病毒。” “我認爲這是我們獲得疫苗的旅程中非常重要的第一步。”
一位不參與Moderna工作的疫苗專家表示,該公司的結果“非常好”。
NIH專家小組成員奧菲特(Paul Offit)說:“這表明該抗體不僅與病毒結合,而且還阻止了病毒感染細胞。”該機構正在爲美國疫苗研究建立框架。

NIH專家小組成員奧菲特
盡管該疫苗在實驗室中取得了令人鼓舞的結果,但尚不清楚它是否能保護現實世界中的人們。
美國食品藥品監督管理局(FDA)已批准該公司開始進行通常涉及數百人的2期臨床試驗,而Moderna計劃于7月開始進行稱爲3期大規模臨床試驗,該試驗通常涉及數萬名患者。
奧菲特說,在大流行之前,疫苗開發商通常會在進入第3期臨床試驗之前在數千人中對其産品進行測試,但是Moderna極不可能在7月份之前接種那麽多人,因爲到目前爲止他們只接種了數十人。
他說,因爲Covid-19每天要殺死數千人,對Moderna來說,沒有給很多人接種疫苗(跳過2期臨床試驗)而直接進入3期臨床試驗是有意義的。






























