默克公司新研發的首款口服抗新冠病毒特效藥即將被FDA批准上巿
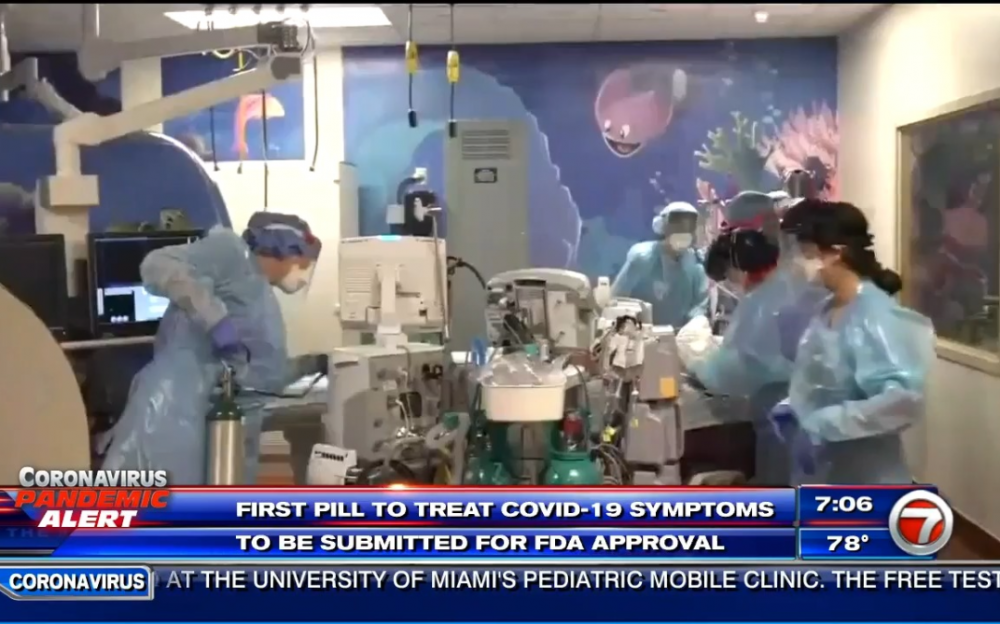
【美南新聞泉深】默克公司( Merck)和 Ridgeback Biotherapeutics公司周五宣布,他們共同開發的的口服抗新冠病毒藥物莫努匹拉韋( molnupiravir)3期臨床試驗結果顯示,可以將輕度或中度新冠患者的住院或死亡風險降低約50%。默克公司表示,監測數據的獨立專家委員會建議提前終止試驗,因爲這個藥物對患者的益處非常明顯,FDA也已同意這一決定,默克公司正等待FDA批准上市。


在該藥物在臨床試驗中顯示出“令人信服的結果”後,默克公司表示將盡快向美國和世界各地的衛生監管機構申請使用授權。
莫努匹拉韋是一種抗病毒藥物,口服給藥,通過抑制新冠病毒在體內的複制而起作用。如果獲得批准,莫努匹拉韋將成爲第一個用于 COVID-19病毒感染的口服特效藥。
目前在美國已獲得授權的所有其它抗新冠病毒療法的藥物都需要靜脈注射,例如之前已經被全面批准的另一款抗病毒藥物瑞德西韋( remdesivir)需要在醫院通過靜脈注射給藥。相比之下,可以在家服用的莫努匹拉韋藥丸將緩解醫院的壓力,也可以幫助遏制世界上較貧窮和較偏遠地區的疫情爆發,這些地區無法獲得更昂貴的輸液治療。
這項3期研究的臨床中期分析發現,在29天內,只有7.3%的患者在接受莫努匹拉韋治療後住院,而在接受安慰劑的患者中,14.1%患者需要住院。在29天內,接受莫努匹拉韋治療的患者沒有報告死亡而接受安慰劑治療的患者有8人死亡。
所有775名試驗參與者都是實驗室確診的有症狀的 COVID-19 患者,並在出現症狀的5天內隨機給予莫努匹拉韋或安慰劑。
所有參與者都沒有接種疫苗,並且有至少ー個潛在因素使他們有更大的風險發展爲更嚴重的症狀,最常見的風險因素包括60歲以上的肥胖者或患有糖尿病或心髒病。
該藥物的3期臨床試驗在美國、巴西、意大利、日本、南非、台灣和危地馬拉等國家和地區的170多個地點進行。
研究表明,莫努匹拉韋的療效不受症狀出現時間或患者潛在危險因素的影響。試驗還證明莫努匹拉韋在治療新冠病毒的所有變種方面始終有效,包括已廣泛和高度傳播的Deltal變異體。
莫努匹拉韋組和安慰劑組的副作用是相當的,大約有10%的莫努匹拉韋治療者報告有副作用,而安慰劑組有13%。莫努匹拉韋組患者因副作用而中止治療低于安慰劑組患者約3.4%。
默克公司還在進行另一項莫努匹拉韋的全球3期臨床研究,以評估其在防止COVID-19 在家庭成員中傳播方面的功效。






























