美国 FDA 允许扩大使用百时美施贵宝细胞疗法 Abecma 治疗血癌

【美南新闻泉深】美国食品和药物管理局(FDA)周五允许使用百时美施贵宝 (Bristol-Myers Squibb)公司和2seventy Bio 公司的细胞疗法Abecma 治疗受影响较轻的血癌患者。
这一决定是在专家顾问小组投票支持使用 Abecma 作为多发性骨髓瘤(一种影响老年人的常见癌症)的早期治疗方法之后做出的。 该细胞疗法已在美国获得批准,用于治疗先前接受过四种或更多疗法的多发性骨髓瘤患者。
卫生监管机构还在审查治疗癌症的其它细胞疗法,为强生公司和其合作伙伴传奇生物技术(Legend Biotech)的细胞疗法 Carvykti 打开了新选项卡,该疗法用于治疗受影响较轻的患者。 FDA 于 4 月 5 日做出决定。
Abecma 和 Carvykti 属于一类称为嵌合抗原受体 (CAR) T 细胞疗法,简称CAR-T 疗法,通过修改称为 T 细胞的淋巴细胞来攻击癌细胞。
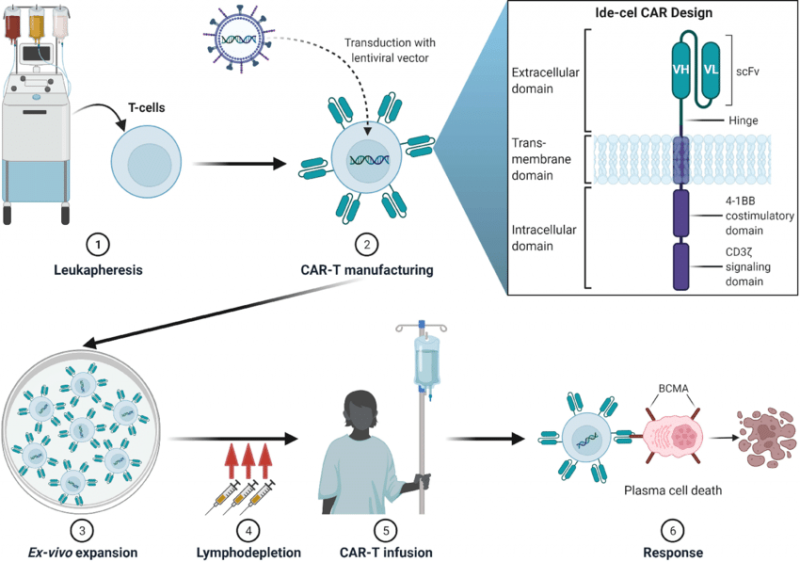
百时美施贵宝的申请包括后期数据,显示 Abecma 有助于将癌症复发或对至少两种先前治疗不再有反应的患者疾病进展前的时间平均延长 13.3 个月。 相比之下,接受标准护理的试验患者的无进展生存期为 4.4 个月。
根据 LSEG 数据,分析师预计 2024 年 Abecma 的销售额将达到 6.01 亿美元。
目前的血癌护理标准包括对受影响较轻的患者使用非 CAR-T 疗法或其它方案,批准治疗这种疾病的药物包括强生公司的达雷木单抗(Darzalex)和非专利抗癌药物,如泊马度胺(pomalidomide)和硼替佐米(bortezomib)。
最近,CAR-T 疗法因继发性癌症的风险而受到卫生监管机构的审查,这种经过基因工程改建后的T淋巴细胞癌变风险较高。 今年早些时候,《自然医学》杂志在报告治疗后出现 T 细胞淋巴瘤后,在CAR-T 疗法的处方信息中添加了安全警告。
泉深微信号:Lionchu888






























